- Líneas I+D+i
- Servicios Tecnológicos
- Servicios Consultoría
- Servicios Laboratorio
- Formación y Eventos
- Sectores

La mejora genética de especies agronómicas es una práctica que lleva en uso desde que se estableció la agricultura sedentaria. En aquellos momentos los agricultores ya elegían qué plantas tenían caracteres deseables y las cruzaban entre ellas para ir, lentamente, generación a generación, derivando su genética hacia cultivos más útiles para el uso humano. Estas prácticas han sido las responsables de poder consumir infinidad de frutas y hortalizas nutricionalmente mejoradas y libres de tóxicos en la actualidad.
Aunque, la mejora genética clásica es un sistema conspicuo y muy útil, la falta de conocimiento genético de las especies, la falta de precisión al no saber exactamente qué está pasando cuándo se llevan a cabo esos cruces entre especies, y, en definitiva, la falta de control, muestran las debilidades de un sistema cada vez menos adecuado para cubrir las necesidades de la sociedad futura. Y es que, el incremento exponencial de la población mundial, los ambientes desfavorables y patrones climáticos anormales derivados de un calentamiento global en alza ponen estos sistemas de mejora contra las cuerdas, y urgen procesos más rápidos y precisos para llevar a cabo estas mejoras en las variedades agronómicas, tan necesarias para la alimentación humana.
En este contexto, los expertos en ingeniería genética llevan décadas creando métodos y diseñando herramientas genéticas para poder acelerar estos procesos, porque al final, de lo que se trata es de reconducir las características favorables de las plantas, hacerlas más resistentes a plagas, aumentar su calidad nutricional, etc., de la manera más rápida y controlada posible.
Gracias a estas herramientas, simples pero complejas a la vez, el genoma se puede editar como si de un texto se tratara. En ocasiones, es necesario “noquear” genes (suprimir la expresión) para obtener el resultado esperado, y otras veces es suficiente con bajar o subir el volumen de estos para redirigir los flujos de una ruta metabólica determinada.
Para empezar, es importante enfatizar que el descubrimiento de esta técnica no hubiera sido posible sin la perseverancia y la pasión por la ciencia de Francis Mojica, un científico de la Universidad de Alicante. Al comienzo de su carrera científica, Francis estudiaba la genética de microorganismos halófilos aislados en las salinas de Santa Pola. Para ello, secuenciaban fragmentos de su genoma en busca de los genes responsables de esa tolerancia a la salinidad y, al estudiar estos genomas, detectó unas secuencias repetidas, que al parecer se habían descubierto también en otros, pero que se desconocía su función.
A Francis, estas secuencias repetidas o “en tándem” le llamaron la atención y junto con otro microbiólogo, R. Jansen, descubridor de los genes que las codifican, las bautizaron como CRISPR (clustered regularly interspaced short palyndromic repeats). Y a los genes adyacentes a estas regiones CRISPR los llamaron Cas (CRISPR-associated).
Tras un tiempo tratando de dilucidar la función “oculta” de estas secuencias, Francis, se percató de que tenía que ver con el sistema de inmunidad adaptativa de procariotas. Y es que resulta que las secuencias o spacers que hay entre las secuencias CRISPR pertenecen a fragmentos pequeños del genoma de virus bacteriófagos. Cuando un virus bacteriófago infecta una bacteria, la bacteria trocea su genoma e incorpora algunos de esos fragmentos en este array. Cuando pasado el tiempo, el mismo tipo de virus infecta a la bacteria, ésta, mediante la proteína Cas9, reconoce al virus (ya que lo recuerda gracias a esos fragmentos que incorporó en el pasado), y lo destruye.
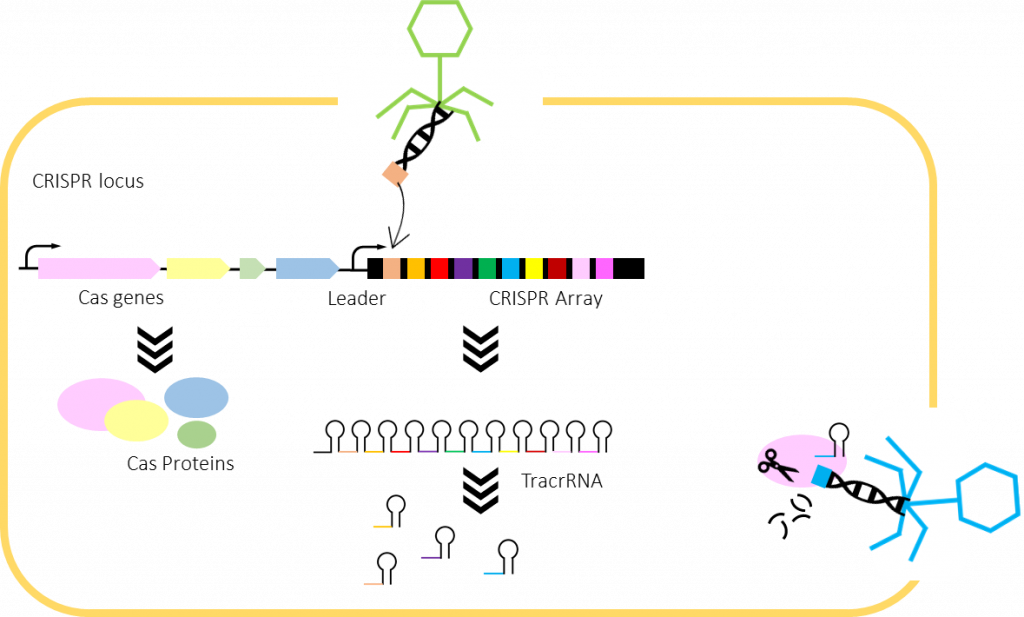
Este sistema adaptativo, que a priori no parecía llevar a ningún lado más que a la pura satisfacción del descubrimiento científico, resultó ser el preludio de una revolución científica.
Crispr-Cas9, la herramienta clave para la edición genética en la Industria Alimentaria
Cas9, además de ser una endonucleasa capaz de cortar ADN de doble cadena, funciona como si de un buscador de secuencias se tratara. Y si sustituimos las secuencias de ADN viral por secuencias del gen que queremos editar, la cas9 lo buscará y lo cortará. Seguidamente, el mecanismo celular reparará el corte, equivocándose en algunas ocasiones y estas equivocaciones son las que romperán la pauta de lectura del gen, inactivándolo.
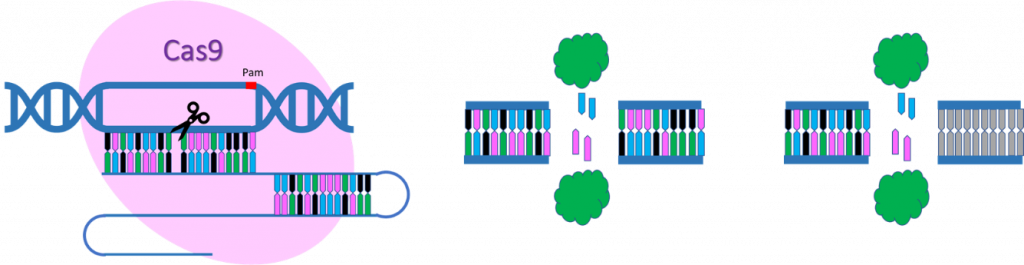
Como hemos mencionado antes, CRISPR-Cas9 sirve para “noquear” o inactivar genes por completo, pero, por otro lado, también sirve para regular la expresión génica o, dicho de otra manera, para activar o reprimir genes. Para esto debemos trabajar con una Cas9 mutada (dCas9), que ya no posee actividad endonucleasa, pero manteniendo su capacidad de “buscador”. Además, para poder llevar a cabo la activación o represión, la Cas9 debe ir acoplada a reguladores de la expresión génica (activadores o represores transcripcionales).
Esta versatilidad proporciona a CRISPR-Cas9 con un grandísimo potencial en multitud de aplicaciones como:
Resulta llamativa la variedad de planteamientos legislativos que hay a nivel internacional en torno a la regulación de estas técnicas, que se encuentran englobadas en lo que llamaríamos las Novel Genomic Techniques (NGT).
En Canadá y en EEUU, por ejemplo, a la hora de regular los productos, no interesa tanto la técnica empleada, sino el rasgo introducido (en el caso de Canadá) o las características del producto, independientemente de si está modificado o no (en EEUU). Por otro lado, en Brasil y Argentina, se basan en la definición del protocolo de Cartagena, que indica que si no hay material genético no es necesario llevar a cabo una regulación específica en ese producto, algo similar a lo que ocurre en Japón, Australia e India, países en los que las NGTs sí que están permitidas.
Sin embargo, la Unión Europea enmarca las NGT en la legislación que regula los Organismos Modificados Genéticamente (OGM), que engloba todas las modificaciones del material genético que no ocurren naturalmente. Esta normativa presenta ciertas exclusiones en técnicas de mutagénesis con historial de uso seguro anterior a 2001, fecha en la que se escribió la normativa.
CRISPR-Cas9 no deja de ser un tipo de mutagénesis, si acaso, diferente de la mutagénesis tradicional en su precisión y control del producto, sin embargo, el tribunal de Justicia en 2018 se acogió al hecho de que las técnicas de edición genética no poseen historial de uso seguro anterior a 2001, y por lo tanto no las incluyó en dicha excepción, quedando reguladas como se menciona anteriormente, en el marco regulatorio de los OMGs.
Afortunadamente, esta decisión se revisará próximamente, ya que en 2019 se adoptó una comisión del consejo en la que se realizará un estudio para decidir o no si se adopta una propuesta legislativa. Este estudio, con fecha límite en abril de 2021 incluirá un informe sobre la situación actual de la aplicación de la legislación sobre productos obtenidos por NGTs y sobre el estado y utilización de estos productos en la UE y otros países. Aunque la primera versión de la EFSA se encuentra disponible, la decisión formal no se conocerá hasta finales de 2021. La decisión que se tome condicionará el posicionamiento de la UE en esta nueva y excitante etapa de la agricultura, en cuanto a la utilización de las NGTs, más controladas y adaptadas a los requerimientos de la sociedad actual.
¿Por dónde empezar? Colaboramos contigo para hacerte evolucionar
Disponemos de conocimiento científico y tecnológico, así como amplia experiencia en la mejora de especies agronómicas. Te acompañamos desde el inicio:

Esta tecnología de edición genética dirigida te permitirá mejorar la productividad y calidad de tus cultivos de una manera rápida y eficaz.
Si estás interesado en cualquiera de estos temas, puedes consultar el vídeo del webinar que organizamos, junto a BIOVEGEN, sobre herramientas de ingeniería genética para utilización en el sector agroalimentario.
Más información es este artículo técnico publicado en «Plant Synthetic Biology»: Design of Multiplexing CRISPR/Cas9 Constructs for Plant Genome Engineering Using the GoldenBraid DNA Assembly Standard
Paloma Juárez (10 artículos)


| Responsable | AINIA |
| Domicilio | Calle Benjamín Franklin, 5 a 11, CP 46980 Paterna (Valencia) |
| Finalidad | Atender, registrar y contactarle para resolver la solicitud que nos realice mediante este formulario de contacto |
| Legitimación | Sus datos serán tratados solo con su consentimiento, al marcar la casilla mostrada en este formulario |
| Destinatarios | Sus datos no serán cedidos a terceros |
| Derechos | Tiene derecho a solicitarnos acceder a sus datos, corregirlos o eliminarlos, también puede solicitarnos limitar su tratamiento, oponerse a ello y a la portabilidad de sus datos, dirigiéndose a nuestra dirección postal o a privacy@ainia.es |
| Más info | Dispone de más información en nuestra Política de Privacidad |
| DPD | Si tiene dudas sobre como trataremos sus datos o quiere trasladar alguna sugerencia o queja, contacte al Delegado de protección de datos en info@businessadapter.es o en el Formulario de atención al interesado |
Consiento el uso de mis datos personales para que atiendan mi solicitud, según lo establecido en su Política de Privacidad
Consiento el uso de mis datos para recibir información y comunicaciones comerciales de su entidad.
